Lê Quốc Tuấn*, Nguyễn Thị Lệ**, Phùng Trung Hùng ***
(* Trường Đại học Y Dược TP. HCM, ** Trường Đại học Văn Lang, *** Đại học Quốc Gia TP. HCM)
---------
Hiện nay, coronavirus 2 (SARS-CoV-2), được đặt tên bởi Tổ chức Y tế Thế giới (WHO), đã trở thành đại dịch toàn cầu nói chung cũng như Việt Nam nói riêng, có xu hướng gây ra tình trạng tổn thương đa cơ quan trên người bệnh, chứ không chỉ riêng tổn thương phổi. Virus SARS-CoV-2 xâm nhập vào tế bào chủ thông qua thụ thể là men chuyển angiotensin 2 (ACE2). Sau đó, chính hiện tượng thực bào virus thông qua đại thực bào sẽ làm lây lan virus đến các tế bào khác có biểu hiện men ACE2 và dẫn đến tổn thương đa cơ quan. Trong cơ thể, men ACE2 có vai trò xúc tác chuyển đổi angiotensin II thành angiotensin-(1–7), và trục ACE2/angiotensin-(1–7)/MAS sẽ giúp cơ thể chống lại các tác động bất lợi từ hệ thống renin-angiotensin (RAS), nhằm duy trì các chức năng sinh lý bình thường. Do đó, việc khôi phục lại sự cân bằng giữa hệ RAS và hệ ACE2/-angiotensin (1–7)/MAS có thể giúp làm giảm các tổn thương đa tạng sau khi nhiễm virus. Đồng thời, các gai glycoprotein của virus phục vụ cho quá trình gắn kết với ACE2 có thể sẽ trở thành mục tiêu tiềm năng để phát triển các loại thuốc đặc hiệu, kháng thể và vaccine cho các chiến lược điều trị sắp tới.
Keyword: Severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2), angiotensin-converting enzyme 2 (ACE2).
SARS-CoV-2 có khả năng lây lan nhanh hơn nhiều so với các anh em khác như SARS-CoV (severe acute respiratory syndrome coronavirus) hoặc MERS-CoV (middle east respiratory syndrome coronavirus). Virus SARS-CoV-2 có trình tự bộ gen giống với virus SARS-CoV đến 79,5%, và cũng xâm nhập vào tế bào chủ thông qua thụ thể là enzym chuyển đổi angiotensin 2 (ACE2) [1]. Chính vì vậy, Tổ chức Y tế Thế giới (WHO) đã quyết định đổi tên virus này từ 2019-nCoV thành SARS-CoV-2. Tính đến nay, tỷ lệ tử vong do SARS-CoV-2 gây ra thấp hơn so với hai người anh em SARS-CoV và MERS-CoV, tuy nhiên tình trạng tổn thương đa tạng lại phổ biến hơn trong các ca bệnh nặng. Vấn đề này được cho rằng có liên quan đến men ACE2, một enzym chuyển đổi angiotensin biểu hiện tại nhiều mô và cơ quan trong cơ thể con người với nhiều hoạt động sinh học quan trọng khác nhau [2, 3].
Hệ thống RAS và trục ACE2/-angiotensin (1–7)/MAS trong cơ thể bình thường
Trong một cơ thể bình thường, hệ RAS (renin angiotensin system) đóng vai trò quan trọng trong việc duy trì huyết áp cũng như cân bằng dịch và điện giải [4]. Từ lâu, giới y sinh học đã biết về hệ thống RAS, trong đó angiotensinogen do gan tiết ra, tiếp theo men renin từ thận phân cắt angiotensinogen thành angiotensin I, sau đó men chuyển ACE từ phổi tiếp tục loại bỏ hai acid amin của angiotensin I và tạo ra angiotensin II. Có ít nhất hai loại thụ thể angiotensin II tại mô đích đã được xác định, trong đó thụ thể angiotensin típ 1 (AT1R) có tác dụng gây co mạch, tăng sinh tế bào, phản ứng viêm, đông máu và tái cấu trúc chất nền ngoại bào. Trái lại, thụ thể angiotensin típ 2 (AT2R) có các tác dụng hoàn toàn đảo ngược với thụ thể AT1R. [5]. Vào năm 2000, lần đầu tiên, giới khoa học đã phát hiện ra ACE2, một chất tương đồng với ACE, có vai trò phân cắt angiotensin II thành angiotensin-(1-7) [2]. Phân tử angiotensin-(1–7) gắn kết lên thụ thể MAS tại mô đích và tạo ra những tác dụng ngược lại với angiotensin II [3].
Phân tử ACE2 và quá trình nhiễm SARS-CoV-2
Sự xâm nhập vào tế bào vật chủ là bước đầu tiên của quá trình lây nhiễm virus. Nhiều công trình đã chỉ ra rằng phân tử ACE2 chính là thụ thể tế bào dành cho SARS-CoV [1]. Các nghiên cứu còn cho thấy ái lực liên kết giữa các gai glycoprotein trên bề mặt SARS-CoV-2 và phân tử ACE2 trên tế bào chủ cao hơn 10-20 lần so với người anh em SARS-CoV [6]. Sau khi sự gắn kết diễn ra, toàn bộ phân tử hoặc hoặc phần xuyên màng của ACE2 sẽ cùng virus xâm nhập vào bên trong tế bào. Tiếp theo, RNA của virus SARS-CoV-2 được phóng thích vào tế bào chất, tạo ra “tế bào nhiễm” [7]. Trong quá trình xâm nhập của virus, vị trí hoạt động xúc tác của men ACE2 không bị giới hạn hay ảnh hưởng [7].
Men ACE2 có mặt tại hầu hết các cơ quan trong cơ thể người. Trên hệ hô hấp, men ACE2 biểu hiện chủ yếu trên bề mặt các tế phế bào típ II, số ít hơn trên biểu mô niêm mạc miệng, mũi và vòm họng. Như vậy, phổi chính là mục tiêu tấn công quan trọng của virus SARS-CoV-2 [8]. Ngoài ra, ACE2 còn được tìm thấy khá nhiều tại tế bào cơ tim, ống lượn gần của thận, biểu mô bàng quang, và các tế bào ruột non, nhất là hồi tràng [8]. Virus sau khi bị thực bào bởi đại thực bào sẽ có khả năng lan truyền từ phổi đến các cơ quan có biểu hiện men ACE2 với mật độ cao thông qua hệ thống tuần hoàn.
Phân tử ACE2 liên quan đến tổn thương đa tạng trong COVID-19
Hầu hết các bệnh nhân COVID-19 nặng đều biểu hiện tổn thương đa cơ quan, bao gồm tổn thương phổi cấp, tổn thương thận cấp, tổn thương tim, rối loạn chức năng gan và tràn khí màng phổi [9]. Tương tự như SARS-CoV và SARS-CoV-2, tổn thương cơ quan nội tạng cũng thường được phát hiện ở những ca nhiễm MERS-CoV, nhất là tại đường tiêu hóa và thận, tuy nhiên tỷ lệ tổn thương tim cấp lại ít phổ biến hơn. Lý do có thể được giải thích là vì MESR-CoV sử dụng DPP4 làm thụ thể xâm nhập tế bào chủ, thay vì sử dụng ACE2 như SARS-CoV và SARS-CoV-2. Phân tử DPP4 biểu hiện chủ yếu trên các phế bào, tế bào biểu mô đa nhân, tế bào tuyến dưới niêm mạc phế quản, bạch cầu hoạt hóa, biểu mô của thận và ruột non,... nhưng DPP4 lại không có mặt nhiều trên các tế bào cơ tim [10]. Như vậy, tình trạng tổn thương cơ quan trong nhiễm virus có mối liên quan chặt chẽ với sự phân bố của các thụ thể xâm nhập trong cơ thể.
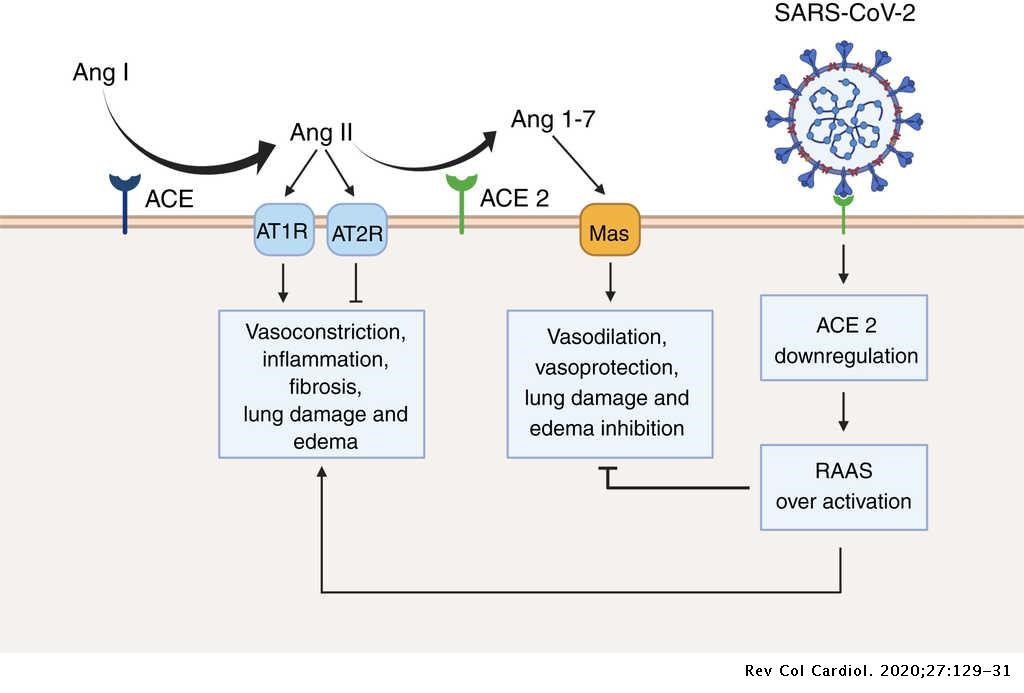
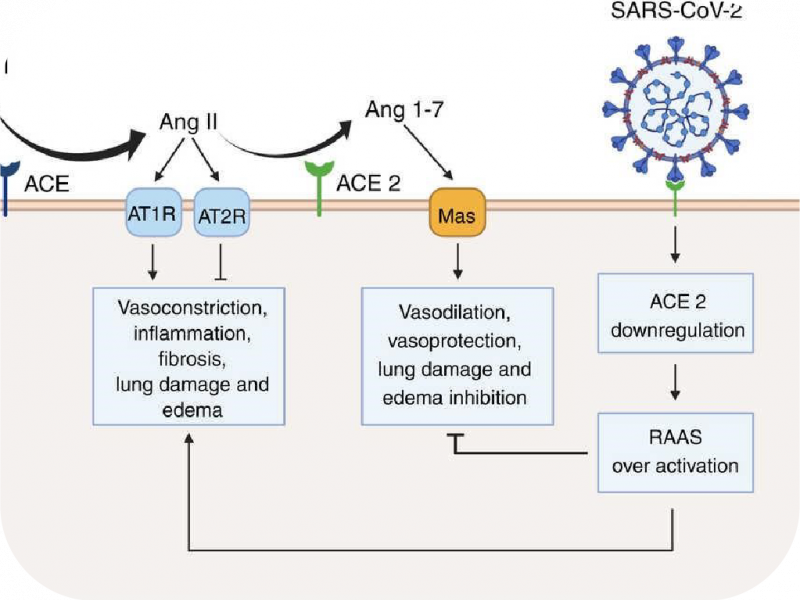
Hình 1. Phân tử ACE2 đóng vai trò là thụ thể cho sự xâm nhập của virus SARS-CoV-2 vào tế bào chủ ở người
Cơ chế phản ứng viêm do virus gây ra trong COVID-19 rất phức tạp, bao gồm sự biểu hiện quá mức của bão cytokine và chemokine, huy động quá mức các tế bào viêm, đáp ứng interferon không đầy đủ và sự sản sinh các tự kháng thể bất thường [11]. Các cytokine tiền viêm PICs (pro-inflammatory cytokines) và chemokine gia tăng đáng kể nồng độ trong huyết tương ở những bệnh nhân COVID-19 nặng, chẳng hạn như IL-1, IL-6, IL-12, IL-8, MCP-1 (monocyte chemoattractant protein-1) và IP-10 (interferon-gamma-inducible protein 10) [12]. Trong đó, PIC và MCP-1 được ghi nhận tăng lên khá nhiều trong các tế bào có mặt ACE2 bị nhiễm SARS-CoV, gợi ý cơ chế tổn thương qua trung gian miễn dịch tại chỗ do virus [13].
Bên cạnh vai trò là thụ thể cho SARS-CoV và SARS-CoV-2, đối với cơ thể, nhiệm vụ chính của men ACE2 là thủy phân angiotensin II thành angiotensin-(1–7). Hệ thống ACE2-/-angiotensin-(1–7)-/-thụ thể MAS có chức năng kháng viêm và chống lại các tác động bất lợi từ hệ thống RAS ngay tại chỗ, do đó giúp đạt được sự thăng bằng sinh lý, bảo vệ các cơ quan tránh tổn thương [3]. Một số nghiên cứu cho thấy tình trạng nhiễm SARS-CoV có thể dẫn đến hiện tượng điều hòa giảm men ACE2 trên bề mặt tế bào (downregulation), do đó phá vỡ sự cân bằng giữa hệ ACE/angiotensin II/ATR1 và hệ ACE2/-angiotensin-(1–7)/MAS. Tình trạng này xảy ra ngay tại chính các tế bào bị nhiễm, góp phần vào cơ chế gây tổn thương cơ quan nghiêm trọng [14]. Bởi vì cách thức xâm nhập của SARS-CoV-2 cũng thông qua ACE2 như SARS-CoV, do đó nhiều khả năng sự mất cân bằng tương tư cũng có thể xảy ra trong tổn thương đa tạng ở bệnh nhân COVID-19 nặng.
Phân tử ACE2 là vị trí đích tiềm năng cho các liệu pháp điều trị
ACE2 và một số phân tử có liên quan đến quá trình xâm nhập của SARS-CoV-2 chính là những mục tiêu tiềm năng cho việc phát triển các thuốc điều trị COVID-19. Huyết thanh từ bệnh nhân đã khỏi SARS có thể vô hiệu hóa sự xâm nhập của SARS-CoV-2 vào tế bào chủ, do đó các vaccine triển vọng sẽ nhắm vào các protein gai virus gắn kết lên thụ thể ACE2 [15]. Các kháng thể đơn dòng đặc hiệu cho SARS-CoV cũng như kháng thể ACE2-Ig tái tổ hợp đều có khả năng ngăn chặn sự xâm nhập của SARS-CoV-2 [15].
Hiện tượng điều hòa giảm biểu hiện ACE2 tại các cơ quan sau khi nhiễm virus có thể gây rối loạn cân bằng tại chỗ giữa 2 hệ RAS và hệ ACE2/-angiotensin-(1–7)/MAS, góp phần vào cơ chế tổn thương đa tạng trong COVID-19. Do đó, việc sử dụng các thuốc ức chế men chuyển (ACEI), ức chế thụ thể (ARB), ức chế renin hoặc các chất tương tự angiotensin-(1–7) có thể mang lại tiềm năng làm giảm tổn thương cơ quan [16]. Một nghiên cứu cho thấy việc áp dụng ACEI và ARB đã làm giảm đáng kể tỷ lệ tử vong trong 30 ngày ở những bệnh nhân viêm phổi cần nhập viện [17]. Tuy nhiên, một số tác giả cũng lo ngại rằng điều trị bằng ACEI và ARB có thể làm tăng mức độ biểu hiện men ACE2 tại các cơ quan, tạo điều kiện thuận lợi hơn cho hoạt động xâm nhập của virus và làm tăng nguy cơ COVID-19 diễn tiến nặng [18]. Tuy nhiên, hai nghiên cứu đoàn hệ lớn cho thấy việc sử dụng ACEI và ARB không liên quan đến sự gia tăng nhiễm SARS-CoV-2, nhưng lại làm giảm nguy cơ tử vong do mọi nguyên nhân trên các ca nhập viện [19]. Chúng ta cần có thêm các nghiên cứu sâu hơn để đánh giá hiệu quả bảo vệ của ACEI và ARB trong bệnh cảnh COVID-19.
DANH MỤC TỪ VIẾT TẮT
COVID-19: Coronavirus disease 2019
SARS: Severe acute respiratory syndrome
MERS: Middle East respiratory syndrome
SARS-CoV: Severe acute respiratory syndrome coronavirus
SARS-CoV-2: Severe acute respiratory syndrome coronavirus 2
MERS-CoV: Middle East respiratory syndrome coronavirus
ACE2: Angiotensin-converting enzyme 2
RAS: Renin-angiotensin system
AT1R: Angiotensin type 1 receptor
AT2R: Angiotensin type 2 receptor
DPP4: Dipeptidyl peptidase 4
PICs: Pro-inflammatory cytokines
MCP-1: Monocyte chemoattractant protein-1
IP-10: Interferon-gamma-inducible protein-10
ACEI: ACE inhibitor
ARB: Angiotensin II receptor blocker
TÀI LIỆU THAM KHẢO
1. Zhou P, Yang X, Wang X, Hu B, Zhang L, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020;579:270–3.
2. Donoghue M, Hsieh F, Baronas E, Godbout K, Gosselin M, Stagliano N, et al. A novel angiotensin-converting enzyme-related carboxypeptidase (ACE2) converts angiotensin I to angiotensin 1-9. Circ Res. 2000;87:E1–9.
3. Patel S, Rauf A, Khan H, Abu-Izneid T. Renin-angiotensin-aldosterone (RAAS): the ubiquitous system for homeostasis and pathologies. Biomed Pharmacother. 2017;94:317–25.
4. Santos R, Sampaio W, Alzamora A, Motta-Santos D, Alenina N, Bader M, et al. The ACE2/angiotensin-(1-7)/MAS axis of the renin-angiotensin system: focus on angiotensin-(1-7). Physiol Rev. 2018;98:505–53.
5. Wrapp D, Wang N, Corbett K, Goldsmith J, Hsieh C, Abiona O, et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science. 2020;367:1260–3.
6. Kuba K, Imai Y, Ohto-Nakanishi T, Penninger J. Trilogy of ACE2: a peptidase in the renin-angiotensin system, a SARS receptor, and a partner for amino acid transporters. Pharmacol Ther. 2010;128:119–28.
7. Li F, Li W, Farzan M, Harrison S. Structure of SARS coronavirus spike receptor-binding domain complexed with receptor. Science. 2005;309:1864–8.
8. Hamming I, Timens W, Bulthuis M, Lely A, Navis G, van Goor H. Tissue distribution of ACE2 protein, the functional receptor for SARS coronavirus. A first step in understanding SARS pathogenesis. J Pathol. 2004;203:631–7.
9. Yang X, Yu Y, Xu J, Shu H, Xia J, Liu H, et al. Clinical course and outcomes of critically ill patients with SARS-CoV-2 pneumonia in Wuhan, China: a single-centered, retrospective, observational study. Lancet Respir Med. 2020;8:475–81.
10. Raj VS, Mou H, Smits SL, Dekkers DH, Müller MA, Dijkman R, et al. Dipeptidyl peptidase 4 is a functional receptor for the emerging human coronavirus-EMC. Nature. 2013;495:251–4.
11. Gu J, Korteweg C. Pathology and pathogenesis of severe acute respiratory syndrome. Am J Pathol. 2007;170:1136–47.
12. Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020;395:497–506.
13. He L, Ding Y, Zhang Q, Che X, He Y, Shen H, et al. Expression of elevated levels of pro-inflammatory cytokines in SARS-CoV-infected ACE2+ cells in SARS patients: relation to the acute lung injury and pathogenesis of SARS. J Pathol. 2006;210:288–97.
14. Haga S, Yamamoto N, Nakai-Murakami C, Osawa Y, Tokunaga K, Sata T, et al. Modulation of TNF-alpha-converting enzyme by the spike protein of SARS-CoV and ACE2 induces TNF-alpha production and facilitates viral entry. Proc Natl Acad Sci U S A. 2008;105:7809–14.
15. Hoffmann M, Kleine-Weber H, Schroeder S, Krüger N, Herrler T, Erichsen S, et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell. 2020;181:271–80.
16. Gurwitz D. Angiotensin receptor blockers as tentative SARS-CoV-2 therapeutics. Drug Dev Res. 2020. https://doi.org/10.1002/ddr.21656.
17. Mortensen EM, Nakashima B, Cornell J, Copeland LA, Pugh MJ, Anzueto A, et al. Population-based study of statins, angiotensin II receptor blockers, and angiotensin-converting enzyme inhibitors on pneumonia-related outcomes. Clin Infect Dis. 2012;55:1466–73.
18. Fang L, Karakiulakis G, Roth M. Are patients with hypertension and diabetes mellitus at increased risk for COVID-19 infection? Lancet Respir Med. 2020. https://doi.org/10.1016/S2213-2600(20)30116-8.
19. Mehta N, Kalra A, Nowacki AS, Anjewierden S, Han Z, Bhat P, et al. Association of use of angiotensin-converting enzyme inhibitors and angiotensin IIreceptor blockers with testing positive for coronavirus disease 2019 (COVID-19). JAMA Cardiol. 2020. https://doi.org/10.1001/jamacardio.2020.1855.




Hãy là người bình luận đầu tiên